Uitgelicht
Bijzondere boorchemie kan nu ook enzymatisch
Groningse onderzoekers hebben een boorzuurvariant in een enzym gebouwd; een primeur in de wereld van de designerenzymen. Daarmee kun je op een ‘natuurlijke’ manier niet-natuurlijke reacties uitvoeren, schrijven ze in Nature.
Opinie
Volgens hoofdredacteur Esther Thole is het hoog tijd dat chemici zich ook mengen in discussies die het moleculaire niveau ontstijgen.
‛We zitten in een heel steile leercurve’
Microplastics houden de gemoederen flink bezig. Zelfs in ons bloed blijken ze inmiddels te zitten, zo liet Marja Lamoree enkele jaren geleden als eerste zien. ‘Onze leefstijl is moeilijk duurzaam te maken.’
Grenzeloos onderzoek met Rubiconbeurzen
De derde en laatste ronde van de Rubiconbeursaanvragen van 2023 zijn eind april uitgedeeld aan zeventien jonge wetenschappers, die met de financiering een onderzoeksproject in het buitenland kunnen volgen.
Moleculen beter vasthouden voor je kwantumcomputer
Breng je ultrakoude moleculen in verschillende kwantumtoestanden, dan kun je optical tweezers veel nauwkeuriger laden. Het brengt de kwantumcomputer een stap dichterbij, aldus onderzoekers uit Nijmegen.
Erkenning voor klimaatinnovatie
Op dinsdag 16 april, tijdens de Antwerp Innovation Night, werden de AHA!-awards 2023 uitgereikt aan de meest innovatieve onderzoekers en bedrijven uit Antwerpen. De winnaars van dit jaar, die overigens geen onbekenden zijn voor C2W | Mens & Molecule, werken allemaal op het gebied van klimaatinnovatie.
Vingervlug werken in de gloed van een hot cell
Door gebruikte brandstoffen te zuiveren en weer op te werken, kan de hoeveelheid radioactief afval. C2W | Mens & Molecule mocht meelopen in het streng beveiligde NRG Hot Cell-laboratorium.
Het multifunctionele schoollab heeft de toekomst
Van klassikale lessen tot practicum, van scheikunde tot drama. In het futuristische schoollab gebeurt van alles. Meer vakoverstijgend onderwijs is de trend, volgens Waldner Benelux, leverancier van laboratorium- en schoolinrichtingen.
Plasmareactor in strijd tegen ammoniakemissies
Om te voorkomen dat ammoniak uit veestallen in de atmosfeer komt, worden luchtwassers toegepast. Een nieuw systeem dat gebruik maakt van een plasma-reactor maakt de stikstofeconomie in varkensstallen circulair.
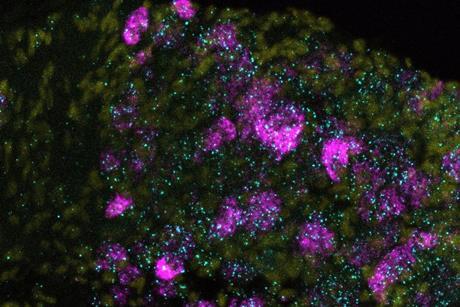
Mass spectrometry innovations in spatial biology
High Purity Day keert terug op Kasteel Maurick
Prof.dr. Peter Schoenmakers (UvA): slot keynote speaker at Analytical Solutions
LIMS: uw volgende stap in de laboratorium automatisering
We can announce the first keynote speaker of Lab Technology 2024!
Lab Technology 2024: Explore the future of laboratory research
Analytical Solutions: een nieuw congres voor Analytische Wetenschappen
- Previous
- Next
- Previous
- Next
Oplossen biedt oplossing
Voor technische kunststoffen, of engineering plastics, wordt closed loop recycling steeds belangrijker. Maar vaak bevatten deze materialen ongewenste componenten, waardoor hoogwaardig hergebruik wordt belemmerd. ReSolved Technologies ziet de oplossing in het letterlijk oplossen van de afvalstromen. ‘Wij denken dat de markt er nu klaar voor is.’
Supersnelle analyse zonder gedoe
De DART-ionenbron maakt targeted MS-analyse veel eenvoudiger, doordat de gebruikelijke chromatografiestap niet meer nodig is. ‘Denk 17 seconden per sample, in plaats van de gebruikelijke 5 tot 10 minuten.’
LIMS houdt alles in de gaten
Diergeneesmiddelenproducent Dopharma koos voor LabWare als leverancier van hun nieuwe laboratory information management system. ‘Het is echt te veel geworden om dit zelf bij te houden.’
Oplichtend perovskiet maakt lood zichtbaar
Start-up Lumetallix biedt een eenvoudige testkit die loodsporen overal betrouwbaar en snel zichtbaar maakt. En dat dankzij een verrassende ontdekking uit oorspronkelijk zonnecelonderzoek.
Ons Kent Ons 2024
Wie heeft er een prijs gewonnen? Wie kreeg die subsidie? Of wie heeft er een nieuwe positie gekregen? In Ons kent Ons houden we je op de hoogte van deze personalia.
Ook nieuws voor onze rubriek? Mail dan naar oko@kncv.nl
Gevoelige kanalen
Kinderproefje voor volwassenen
Oerwoud in een kolf
Evolutie van een mesosfeergeest
Kralenparade
- Previous
- Next
Sprekers Avond van de Chemie bekend!
Save the date: FEBS 2026 conferentie in Maastricht
NVBMB Prijs 2024
H.G.K. Westenbrinkprijs 2022 - 2023
Plant Genomics symposium & NBV-netwerkdiner tijdens ECB
- Previous
- Next
Grenzeloos netwerken
Verre afstanden zijn voor Kimberly Tran (23) geen belemmering om een indrukwekkend internationaal netwerk op te bouwen. ‘Ik vind het interessant om te zien hoe chemie er buiten Nederland uitziet.’
Podium: Maarten Merkx
Onze leden geven de chemie en life sciences kleur en betekenis; wie zijn zij? Deze maand op het podium: NVBMB-lid Maarten Merkx.
Steeds vaker
Kijk goed naar de cijfers achter een verhaal, waarschuwt Enith Vlooswijk. Zonder verdere context kun je percentages en getallen niet goed duiden.
‘Geen nieuwe academische samenwerkingen met fossiele bedrijven niet gecommitteerd aan Parijs’
Fossiele bedrijven geven voorrang aan de kortetermijnbelangen van hun aandeelhouders en werken zo de energietransitie tegen. Voor universiteiten is samenwerking met deze partijen daarom geen optie, vinden Geert-Jan Kroes en Philipp Gramlich.
Duidelijkheid over dosering voor zwangeren op komst
De effectiviteit en veiligheid van geneesmiddelen voor zwangeren is nauwelijks onderzocht, waardoor over de juiste dosering veel onduidelijkheid heerst. Het eerste gerichte doseeradvies van Moeders voor Morgen Lareb betekent een stap op weg naar betere gefundeerde doseeradviezen voor zwangeren.
Scherper zicht op de kosten van chemisch recyclen
Wie de kosten van een nieuwe chemische plasticrecyclinginstallatie wil inschatten, kan het beste kijken naar energieverlies, blijkt uit recent onderzoek. Mogelijk kan dat simpele gegeven gaan helpen om grootschalige plasticrecycling via de petrochemie vlot te trekken.
In het klimaatbos groeien de bomen niet tot in de hemel
Bedrijven en overheden rekenen zich veel te rijk met plannen voor het afvangen van koolstofdioxide met bosaanplant en energiegewassen, waarschuwen onderzoekers in Science.
Kleinste PFAS: meer mensenhand dan moeder natuur
Trifluorazijnzuur (TFA) wordt volgens sommigen ook in de natuur gevormd. Chemici zijn daar inmiddels niet meer zo zeker van, omdat er twijfels zijn over eerder onderzoek.
Agenda
11th Life Science Symposium
Altering Evolution: Taking the future in our own hands
De chemie achter het bieraroma
Studieavond met Gert De Rouck, Managing Director Pilot Malting and Brewery - EFBT
To bond or not to bond?
Brightlands Polymer Days 2024
Lab Technology 2024
Explore the future of laboratory research
Tatoeages: onschuldige decoratieve trend of gevaar voor de gezondheid?
Avondlezing door ing. D.J. Schakel georganiseerd door de Haarlemse Chemische Kring
Dossier: de sneaker
Sportief en stoer, maar zacht voor je voeten. De sneaker dankt zijn bestaan aan de reactie van zwavel met latex uit de rubberboom. Dat zorgde voor de komst van stevig, elastisch en bijna geruisloos rubber, ideaal voor een sportzool. Met gemiddeld 65 onderdelen en tien verschillende soorten vaak synthetische materialen vormen sneakers helaas ook een grote afvalhoop.
Dossier: anammox
Het begon rond 1990 met een opmerkelijke observatie in een proefwaterzuivering van Gist-Brocades, waar door een onbekend proces stikstofgas werd gevormd. Pas na jaren van volhardend experimenteren door onderzoeksgroepen in Delft en Nijmegen kwamen de eerste anammox-bacteriën in beeld.
Dossier: Cannabis
Cannabisproducten kunnen verlichting brengen bij uiteenlopende aandoeningen en symptomen. Maar gecontroleerd gebruik blijft belangrijk.
Dossier: Zweedse elementen
In dit dossier lees je over de ontdekking, de toepassingen en de uitdagingen van het scheiden van een groep zeldzame aardmetalen die in Zweden zijn ontdekt.
Dossier: Zeolieten
In dit dossier lees je over zeolieten: een speeltuin voor chemici. De industrie gebruikt synthetische zeolieten als ionenwisselaars, katalysators en adsorbens, maar nu we zoeken naar andere grondstoffen, hebben we ook andere zeolieten nodig.
Dossier: Kweekvlees
Eén gram koeienspier, duizenden hamburgers: kweekvlees is misschien wel de meest ambitieuze en kansrijke vleesopvolger van allemaal. De voordelen ten opzichte van de bio-industrie zijn in potentie enorm, maar heeft de consument er ook trek in?
-
Senior Laborant Chemie - Haarlem
-
Application Specialist Field Sales Petrochemical Meetsystemen Instruments - Delft
-
Chemisch Procestechnoloog - Roermond
-
Application Specialist Field Sales Petrochemical Meetsystemen Instruments - Rotterdam
-
Application Specialist Field Sales Petrochemical Meetsystemen Instruments - Rotterdam
-
Opgelet Chemicus of Laborant word Procesoperator - Oss
-
(Global Petrochemical) Research Scientist Lead - Amsterdam
-
Zij-instroom docent scheikunde - Apeldoorn
Stephan Hacker – Zoektocht naar zwakke plekken in bacteriën
Maurits de Roo – Chemische reacties met elektriciteit in plaats van chemicaliën
Pascal Vermeeren – Chemische mysteries ontrafelen met nieuwe modellen
Nico Claassens – Producten van de toekomst maken uit CO₂ met bacteriën
Tassos Perrakis – Eiwitten voor het volk
Alina Chanaewa – Scheuren in koolstofvezelcomposiet detecteren
- Previous
- Next